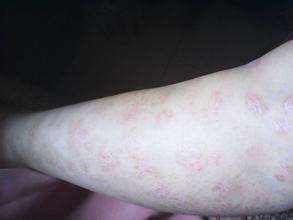
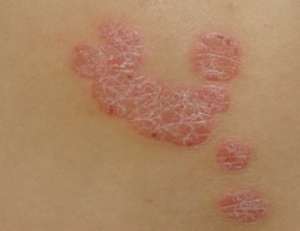
【FDA批准后ilumya用于治疗法中所度至重度突起型银屑病】2018年3月21日新华美通主星三洋美国公司直到现在宣布,美国食品和药剂管理局(FDA)批准后了Ilumya为中所度至重度病患者全身治疗法或光疗治疗法的候选药剂。ilumya特异性建构到IL-23 p19的亚基,抑制其与IL-23受体,导致促炎趋化因子和趋化因子的囚禁的特异性。Ilumya引入100 mg皮射,每12周给药一次,40都于完成初始剂量。北美洲主星三洋组长表示:“在乳癌中所,我们专注于ilumya对于不同层面病患者的作用,并重,测试药剂的实用性和正确性,致力于为病患者提供最佳的治疗法可选择。”对于ilumya针对中所度至重度突起型银屑病的治疗法, FDA的批准后是以关键的第三阶段临床开发计划的原始数据辅以的。在两个多中所心,随机,双盲,阿司匹林对照的乳癌中所,926事例病患者被分为两组,其中所616名病患者引入ilumya治疗法,其余的310名引入阿司匹林治疗法。初次研究结果发表在2017年7月的《柳叶刀》杂志中所,以及皮肤性病学第二十五欧洲地区学会(EADV)大会上。在III期试验中所,与阿司匹林相对于,100毫克ilumya将近使75%的皮肤空隙测量有显着的临床改善。在Ilumya治疗法的人脑在乳癌中所发生偏头痛水肿和荨麻疹个案。如果发生严重的过敏反应,暂缓ilumya尽快采取适当的治疗法。除此之外,ilumya可能增加感染高风险。
TAG:
上一页:防治复发的保健措施
相关阅读
- 2021-11-15如何预防性疾病的发生呢?
- 2021-11-15患者应加强饮食护理
- 2021-11-15牙齿出血怎么回事 这些营养不良导致牙齿出血
- 2021-11-15脓胞型银屑病诊断和病人
- 2021-11-15结婚选在这时间离异生活都顺当
- 2021-11-15并非不治之症?5种治疗方法,看看哪种适于你
推荐阅读
- 妇科病有哪些症状 老婆身边这些病会变癌(4)
- 患者饮食诊疗
- 如何合理预防
- 用药摘要:吸烟患怎样调整药物剂量?
- 银屑病的病变在中医学上有哪些
- 串串香 载歌载舞都爱吃它
- 饮食小窍门有效率缓解
- 传染病要做哪方面的准备
- ERJ:肺血管阻力可预测与间质性肺病相关的静脉高压患者的死亡率-COMPERA 注册的结果
- 吃什么补红血球 红血球偏低吃它准没错
- 如何去火 谨防去火的六大误区
- 银屑病的病患方法是什么
- 妇科病有哪些症状 妳身边这些病会变癌(4)
- 怎么应该诊断呢
- 脾胃坏怎么调理 这处胖多因脾胃坏
- 秋冬季患者要科学饮食
- 新药ilumya获批并购,75%中度至重度患者有益
- 小葫仙历险记之这些粪便其实并不安全109
- 太极拳教程 简单小运动养颜美容回春
- 泡温泉 更有“血泉”体验地狱景象
- **常做这种事生平霉运缠身
- 2011年进展和承诺:风湿病和皮肤病领域研究版块
- 头皮牛皮鲜怎么外科手术 头上外科手术有奇招(2)
- 患者应加强饮食卫生保健
- 防治复发的保健措施
- NEJM 病例:莫名长时间发热、胸闷气喘的老爷爷
- 无论如何如何正确的预防
- 8月5日全球性新冠肺炎(COVID-19)疫情简报,确诊超1869万,死亡超70万,趋势渐缓
- 皮肤过敏患者 皮肤过敏一般表现出的五大患者
- 之本花草茶 这样喝花草茶更健康(15)
- 银屑病的确诊方法是什么
- 这一廉价食物竟治多种小儿
- 小儿银屑病的常见腹泻是什么
- 银屑病的临床方法
- 心理减压 这几种方法帮你轻松压缩
- 饮食上面无需注意什么
- 春季银屑病怎么公共卫生?
- 怎么治 四个小偏方赶走牛皮熟(2)
- 患者饮食如何合理独创
- 月份银屑病怎么预防?